Superbugs
Ein selbst verschuldeter Notstand
Das Vordringen von Superbugs, denen Medikamente nichts anhaben können, gefährdet die Wirksamkeit antibiotischer Therapien; aber um dies zu lösen, müssen wir uns nicht nur mit wissenschaftlichen Herausforderungen auseinandersetzen, sondern mit der aktuellen therapeutischen Praxis selbst.
Ein mikrobieller Feind, der mit bloßem Auge nicht sichtbar ist, dürfte bis 2050 jedes Jahr Millionen von Menschenleben und 1,7 Billionen US-Dollar kosten, meldet ein Report der Denkfabrik Center for Global Development. Der Schaden wird nicht durch Krieg, Hunger oder Klimakatastrophen verursacht werden, sondern durch den Siegeszug von Superbugs – Mikroorganismen (vor allem Bakterien), gegen die heutige Therapien wie Antibiotika nicht wirken.
Wie die Klimakrise ist auch antimikrobielle Resistenz (AMR) so komplex, dass sie schwer zu erfassen ist. Sie ist als „stille Pandemie“ bezeichnet worden, als „langsamer Tsunami“ und „Strom aus geschmolzener Lava“. Inzwischen greifen die Flammen der Superbug-Krise an mehreren Fronten um sich. Von vielen Seiten ist Alarm geschlagen worden: Es muss dringend etwas getan werden.
Doch angesichts der erwarteten Schwere dieser Krise ist die dringlichste Frage nicht, ob wir genug wissen, um handeln zu können, sondern warum es so schwierig ist, etwas Nachhaltiges zu tun. An wissenschaftlicher Unkenntnis liegt es nicht. Das größte Hindernis für die Überwindung dieser Gefahr ist die Natur des Menschen selbst – unser kurzfristiges Denken, konkurrierende Interessen und das Fehlen verantwortungsvollen Handelns. Um voranzukommen, müssen wir unsere gemeinsame Verantwortung wahrnehmen und die Begrenztheit von Lösungen anerkennen, die nur auf Wissenschaft beruhen.
Die Kraft, zu heilen
Vor nicht allzu langer Zeit waren bakterielle Infektionen wie Tuberkulose und Diphtherie unter den häufigsten Todesursachen. Moderne wissenschaftliche Entdeckungen haben uns ein Gefühl der Sicherheit vor der Gefahr von Infektionskrankheiten gegeben, besonders für Menschen in wohlhabenden Regionen.
Ein erster Schritt in diese Richtung geschah im späten 19. Jahrhundert mit den bahnbrechenden Pionierleistungen des französischen Chemikers Louis Pasteur und des deutschen Arztes und Biologen Robert Koch in der „Keimtheorie“.
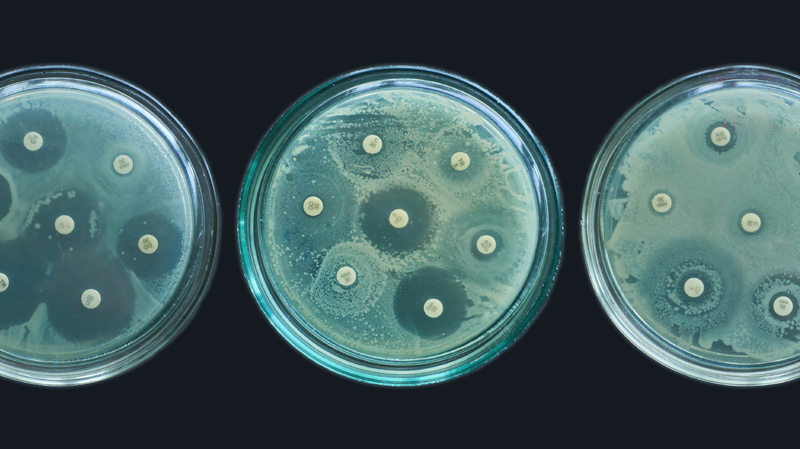
Eine Entdeckung des schottischen Arztes und Mikrobiologen Alexander Fleming schuf 1928 die Voraussetzung, um bakterielle Infektionen zu bekämpfen. Als Fleming in den Sommerurlaub fuhr, ließ er in seinem Labor eine Petrischale mit Staphylococcus-Bakterien in der Nähe eines offenen Fensters stehen. Als er im September zurückkam, hatte ein seltener Stamm luftgetragener Schimmelsporen das Präparat besiedelt: Penicillium notatum. Fleming beobachtete, dass der Schimmel verschiedene Bakterien abtötete, erkannte aber das volle Potenzial seiner Entdeckung nicht und gab das Projekt im Sommer 1929 auf.
Angesichts der drängenden Notwendigkeit im Zweiten Weltkrieg griffen die Oxforder Forscher Ernst Chain und Howard Florey Flemings Entdeckung mehr als ein Jahrzehnt danach wieder auf, um den Schimmel zu reinigen und zur Produktionsreife zu bringen. 1944 bemerkte Winston Churchill zu der Bedeutung von Penicillin während des Kriegs, es sei „just in dem Moment über die Welt hereingebrochen, in dem Menschen in enormen Zahlen auf dem Schlachtfeld von Wunden zerschnitten und zerrissen und vergiftet werden“. 1945 erhielten Chain und Florey gemeinsam mit Fleming den Nobelpreis in Physiologie oder Medizin.
„Dank Penicillin […] wird er heimkommen.“
Interessanterweise war Flemings Entdeckung in bestimmter Hinsicht eine Art Wiederentdeckung. Laut dem Medizinprofessor Matt McCarthy ist bekannt, dass Menschen in der Antike Antibiotika zu sich nahmen, wahrscheinlich in gebrautem Bier, wie sudanesische Mumien von 350–550 n. Chr. erkennen lassen. In der ägyptischen Oase Dakhla gefundene Oberschenkelknochen aus der spätrömischen Zeit enthielten Spuren von Tetracyclin. McCarthy schreibt: „Unsere Vorfahren verstanden die Wirkung von Antibiotika, wenn auch nicht den Mechanismus.“
Warum Flemings Entdeckung trotzdem so bedeutend war, ist eher zu verstehen, wenn man versteht, was Antibiotika tun. Da sie antimikrobiell sind, wirken sie gegen Bakterien. Der Begriff Mikrobe ist breit und umfasst Bakterien, Viren und Pilze. Muhammad H. Zaman, Professor für Biomedical Engineering and International Health an der Boston University, schreibt: „Es gibt mehr Bakterien auf der Erde als Sterne im Universum – rund 40 Billionen im menschlichen Körper allein.“ Die Masse dieser Bakterien entspricht rund 0,3 % unseres gesamten Körpergewichts.
Es ist eine fantastisch ausgewogene Beziehung. Die meisten Bakterien sind für Menschen unschädlich oder nützlich; wir brauchen sie. Wird dieses Gleichgewicht aber gestört, können manche Bakterien Probleme verursachen, je nachdem welchen Teil des Körpers sie besiedeln.
Eine Kraft, die schwindet
Die Entdeckung und Entwicklung von Penicillin war von entscheidender Bedeutung im Kampf gegen bakterielle Erkrankungen. Sie wird oft als Paradebeispiel für eine glückliche Fügung gesehen – die zufällige Entdeckung von etwas höchst Nützlichem.
Doch obwohl Penicillin und andere Antibiotika die Behandelbarkeit bakterieller Infektionen sehr verbesserten, war ihre Wirksamkeit immer gefährdet. Nachdem Fleming den Nobelpreis erhalten hatte, wies er auf den Zusammenhang zwischen einer potenziellen Fehlanwendung und einer künftigen Gefahr steigender Resistenz hin: „Die Zeit kann kommen, in der Penicillin von jedermann im Laden gekauft werden kann“, sagte er. „Dann besteht die Gefahr, dass der Unwissende sich leicht unterdosieren und seine Mikroben resistent machen kann, indem er sie dem Wirkstoff in nicht tödlichen Mengen aussetzt.“ Er schloss mit einer deutlichen Warnung – „Moral: Wenn Sie Penicillin nehmen, nehmen Sie genug.“
Fleming verstand das Risiko, dass Fehlanwendung die Kraft dieses neuen Mittels mindern würde, und genau das ist geschehen. Ob durch ein Zuwenig oder ein Zuviel – wir haben Antibiotika auf unwirksame Weise eingesetzt und dadurch ihre Wirksamkeit geschwächt.
Es ist ein verbreitetes Missverständnis, dass unser Körper resistent gegen Antibiotika wird. Tatsächlich sind es die Bakterien, die sich verändern und so resistent werden, dass die Wirkstoffe nichts mehr gegen sie ausrichten. Wir stehen am Abgrund zu dem, was Margaret Chan, ehemalige Generaldirektorin der Weltgesundheitsorganisation (WHO), als „postantibiotische Ära“ bezeichnet hat.
Projektionen zufolge wird das Problem eine solche Größenordnung erreichen, dass es keine Option ist, es nicht zu lösen. Bei Verfahren wie dem Einsetzen künstlicher Hüftgelenke, Kaiserschnitt und Organtransplantationen müssen zum Schutz der Patienten Antibiotika eingesetzt werden. In einem Worst-Case-Szenario müsste man die Entscheidung, Krebs zu behandeln, gegen das Risiko einer nicht behandelbaren Infektion abwägen.
Wenn die Situation sich so weit verschlechtert, „werden im Wesentlichen die letzten 70, 80 Jahre der modernen Medizin verloren gehen, und wir fallen zurück zu der Ära, bevor Penicillin entdeckt wurde“, so Danilo Lo Fo Wong, leitender Regionalbeauftragter der WHO für die Bekämpfung antimikrobieller Resistenzen in Europa. In der Ära vor Penicillin war die Lebenserwartung weit niedriger als heute. Damals konnte man an einem infizierten Kratzer sterben.
Die Situation hat zu einer bitteren Ironie geführt: Das Krankenhaus – ein Ort, der dazu da ist, Menschen zu heilen, und wo Antibiotika verabreicht werden – ist wahrscheinlich genau der Ort, an dem Superbugs gedeihen. Ein solcher Superbug ist der gefürchtete methicillinresistente Staphylococcus aureus (MRSA), der lebensbedrohlich sein kann. Bei Untersuchungen des Abwassers von einigen Krankenhäusern wurden höhere Belastungen mit gegen Antibiotika resistenten Bakterien gefunden als in den umgebenden Wohngebieten.
„Statt sich selbst zu helfen, hilft die Menschheit derzeit offenbar den Superbugs.“
Doch die Ironien haben begonnen, noch tiefer zu gehen. Der Geophysiker Mihai Andrei hat auf den Superbug Pseudomonas aeruginosa aufmerksam gemacht, der eine Vorliebe für Plastik hat. Andrei berichtet: „Er kann Polykaprolakton (PCL) aufspalten – ein biologisch abbaubares Polymer, das viel in medizinischen Implantaten eingesetzt wird – und es als Kraftstoff nutzen, um stärker zu werden. Das bedeutet, dass in genau den Umgebungen, wo wir geheilt werden sollen, manche Mikroben jetzt lernen könnten, dank der Materialien zu gedeihen, die unseren Körper wiederherstellen sollen.“ Mit anderen Worten: Manche Mikroben sind in ihrer Anpassung schneller als unsere Bemühungen, sie in Schach zu halten; sie gedeihen auf unsere Kosten.
So beunruhigend diese Entwicklungen sind – die Reichweite des Problems endet damit nicht. Es ist eine menschliche Entdeckung in der Hand von Menschen und deshalb so komplex wie wir selbst. In manchen Teilen der Welt sind Antibiotika zum Beispiel frei verkäuflich, was das Risiko des übermäßigen Einsatzes mit der Folge der Unwirksamkeit erhöht. In anderen Teilen der Welt besteht das Problem darin, dass Antibiotika nicht verfügbar sind.
Menschliche Systeme, menschliche Folgen
Gleichzeitig arbeiten Ärzte und Ärztinnen oft unter intensivem Druck. Eine 2022 durchgeführte Befragung in der englischen Ärzteschaft, die in der Fachzeitschrift Medical Decision Making veröffentlicht wurde, ergab, dass der Prozentsatz der Verordnungen von Breitband-Antibiotika um 6,4 % stieg, als dieser Druck zunahm. Breitband-Antibiotika töten oder hemmen ein breites Spektrum von Bakterien. Sie werden in der Regel zur Behandlung bakterieller Infektionen eingesetzt, wenn die Bakteriengruppe unbekannt ist oder die Infektion von mehreren Bakterienarten verursacht wird. Diese wirkmächtigen Mittel sind oft notwendig, aber sie können das bakterielle Gleichgewicht des Körpers stören und die Entwicklung von Resistenzen beschleunigen, da sie mehrere bakterielle Spezies dem Wirkstoff aussetzen.
Das Problem des übermäßigen Einsatzes besteht allerdings nicht nur in der Humanmedizin. In den Jahrzehnten nach Flemings Entdeckung ist eine massenhafte Nutzung von Antibiotika in der Tierhaltung und Fischzucht aufgekommen und nicht nur erkrankte Tiere werden damit behandelt. Bei nur wenig regulatorischer Überwachung wurden sie bald auch zu Vorbeugung gegen Infektionen verabreicht. Forschungsergebnisse zeigten, dass die Gabe von Antibiotika bei manchen Tieren das Wachstum beschleunigt und damit eine intensive Viehwirtschaft ermöglicht. So wurde Flemings Entdeckung zu einer festen Größe für die Wirtschaftlichkeit und den Ertrag in der Landwirtschaft und der Lebensmittelproduktion. Mit Antibiotika können wir so viele Menschen ernähren, wie wir es heute tun, aber nur unter Missachtung der Prinzipien verantwortungsvollen Wirtschaftens und auf Kosten der Wirksamkeit der gleichen Antibiotika für alle.
Dieses Muster – Gewinn auf kurze Sicht zum Preis einer Krise auf lange Sicht – herrscht auch in der pharmazeutischen Industrie selbst. Finanziell wird die Welt des Handels von Angebot und Nachfrage bestimmt. Unternehmen, auch Pharmafirmen, stellen ein Produkt her und treiben dann den Absatz an, um höhere Gewinne zu erzielen.
Aber die Notwendigkeit von Antibiotika für die Gesellschaft folgt nicht dieser profitgesteuerten Dynamik. Infolge der Resistenzen gegen vorhandene Mittel ist die Welt darauf angewiesen, dass neue Antibiotika auf den Markt kommen und dass der unnötige Einsatz beschränkt wird, um weiteren Resistenzen vorzubeugen. Beides ist auf verwickelte Weise in die Komplexitäten von Finanzen und Regierung eingebunden. Angesichts der enormen Investitionen, die erforderlich sind, um einen neuen Wirkstoff bis zur Erprobung zu bringen, hält das Wirtschaftssystem nicht mit dem Schritt, was gebraucht wird, um das Problem zu lösen. Deshalb ist die Produktion neuer antibiotischer Wirkstoffklassen für die Humanmedizin seit der Mitte der 1980er-Jahre weitgehend versiegt.
„Erfolgreiches Vorgehen gegen AMR beruht auf politischem Engagement, nachhaltiger Finanzierung, Erfolgsmessung mit Zuordnung von Verantwortung und vor allem […] dass alle Betroffenen in den Mittelpunkt des Vorgehens gestellt werden.“
Regierungen haben Schritte unternommen, um die Gefahr von AMR bekannter zu machen und Maßnahmen dagegen zu fördern, aber das Dauerproblem politisches Kurzzeitdenken bleibt ein großes Hindernis. Was sofortige, sichtbare Vorteile bringt, hat Vorrang vor langfristiger Planung und nachhaltigen Lösungen.
Noch schwieriger wird die Komplexität der Probleme für Regierungen dadurch, dass die Krise sich weiterentwickelt, und dies weltweit unterschiedlich. Die Herausgeber des Sammelbands Steering Against Superbugs: The Global Governance of Antimicrobial Resistance schreiben: „Die Eindämmung von AMR ist von globaler Bedeutung, aber Strategien für ihre Umsetzung hängen stark davon ab, in welcher Form AMR in spezifischen Regionen, Ländern und sogar spezifischen Orten auftreten.“
Es könnte sein, dass uns die Zeit davonläuft. Einem einflussreichen Bericht zufolge können die jährlichen Sterbefälle im Zusammenhang mit Superbugs bis 2050 schlimmstenfalls ähnlich hoch werden wie die durch Krebs und zehn Millionen erreichen.
Feuerwehr
Die Superbug-Krise spiegelt die Komplexität der menschlichen Systeme, die sie gefährdet – wirtschaftlich, politisch und sozial. Um sie wirksam zu bekämpfen, bedarf es ebenso vielfältiger Lösungen, und dies umfasst nicht nur wissenschaftliche Innovationen, sondern auch die Überwindung der strukturellen Barrieren, die wirksame Maßnahmen behindern.
Eine Möglichkeit, Pharmafirmen Anreize zur Produktion neuer Antibiotika zu bieten, sind Markteintrittsprämien. Mit solchen Programmen können sowohl Unternehmen als auch Regierungen verschiedene Elemente der Entwicklung von Medikamenten in Angriff nehmen. Im Rahmen dieses Systems können Hersteller eines neuen antibakteriellen Wirkstoffs eine Geldprämie erhalten, wenn das Medikament auf den Markt gebracht wird.
Fürsprecher dieses Modells finden, dass es der richtigen Art entspricht, über Antibiotika zu denken. Laut John Rex, einem Kenner dieses Themas, sollte man an Antibiotika ganz ähnlich denken wie an eine Feuerwehr – selten in Anspruch genommen, aber im Bedarfsfall unverzichtbar. Daher sollten sie in ähnlicher Weise finanziert werden. Rex schreibt: „Wenn man Feuerwehrleute bezahlt, bezahlt man sie pro Brand, oder zahlt man ihnen ein Gehalt? Natürlich Letzteres, und wie wichtig es ist, auf der Ebene der Gemeinschaft zusammenzuarbeiten, um eine jederzeit einsatzbereite Feuerwehr zu haben, ist schon seit dem alten Rom bekannt.“
In den USA wurde 2020 erstmals das Gesetz „Pioneering Antimicrobial Subscriptions To End Upsurging Resistance (PASTEUR)“ vorgestellt. Dieses Gesetz zur Beendigung des Anstiegs von Resistenzen würde ermöglichen, dass „das Gesundheitsministerium Subskriptionsverträge für kritisch erforderliche antimikrobielle Medikamente eingeht“, und ein alternatives Finanzierungsmodell mit dem Ziel schaffen, Anreize für die Produktion neuer Antibiotika zu bieten. Kevin Outterson ist Experte für Antibiotikaresistenz und Geschäftsführer von CARB-X (Combating Antibiotic-Resistant Bacteria Biopharmaceutical Accelerator, biopharmazeutischer Beschleuniger im Kampf gegen antibiotikaresistente Bakterien). Er hat gesagt, im Rahmen des PASTEUR-Gesetzes „verdient das Unternehmen das Gleiche, unabhängig davon, wie viel von dem Antibiotikum eingesetzt wird. […] Und wir stellen dieses neue Antibiotikum als Feuerlöscher ins Regal: Wir wollen es erst einsetzen, wenn wir müssen“. Aufgrund von Meinungsverschiedenheiten über einige seiner Elemente ist das Gesetz allerdings noch nicht verabschiedet worden.
Ein weiterer bemerkenswerter Schritt in Richtung einer Lösung war der Vorschlag eines „One Health“-Ansatzes zu Beginn der 2000er-Jahre, dem 2004 die erste „One World, One Health“-Konferenz an der Rockefeller University folgte. Die Konferenz wurde als Erfolg gewertet, weil sie die enge Verknüpfung der „Gesundheit von Menschen, Tieren und Umwelt“ und der Verantwortung dafür anerkannte – ein wichtiger Schritt, weil damit anerkannt wird, dass jede echte Lösung Verantwortung über getrennte, aber verbundene Lebensbereiche hinweg erfordert.
Diese Vernetztheit erfordert sowohl globale als auch regionale Bemühungen um Lösungen. Die Autoren von Steering Against Superbugs sehen, dass „AMR zu beherrschen, gewiss von globaler Koordination und Führung abhängt“. Aber sie merken auch an, dass die Komplexität der AMR-Krise in verschiedenen Teilen der Welt „polyzentrische und ,glokale‘ [globale + lokale] Steuerungsansätze verlangt statt eines nur uniformen, globalen Ansatzes“.
Die wissenschaftliche Innovation geht ebenfalls weiter. Ein vorgeschlagener Lösungsweg nutzt künstliche Intelligenz (KI) zur Verbesserung von Diagnose und Überwachung. Diese Technologie beginnt, Resultate zu bringen. Mithilfe generativer KI sind zwei neue potenzielle Antibiotika erfunden worden, die gegen Gonorrhöe (Tripper) und MRSA wirken könnten. Das Team des Massachusetts Institute of Technology, das sie entwickelt hat, glaubt, KI könnte ein „zweites Goldenes Zeitalter“ der Entdeckung von Antibiotika ermöglichen. Doch obgleich diese Verbindungen, die Atom für Atom von der KI entwickelt wurden, die Superbugs unter Laborbedingungen und in Tierversuchen erfolgreich abtöten konnten, sind diese Entwicklungen von einer breiten klinischen Anwendung noch Jahre entfernt.
Über KI hinaus wird in der Forschung weiter für neue Antibiotika gearbeitet; im Boden werden neue Pathogeninhibitoren entdeckt, Impfstoffe zur Vorbeugung werden entwickelt und Bakteriophagen (oder Phagen [Fresser] – Viren, die selektiv Bakterien infizieren) für die Behandlung krank machender bakterieller Infektionen geschaffen.
Andere Maßnahmen sind niederschwelliger: Verbesserung von Kanalisation, Wasserqualität und Hygiene, wo dies nötig ist, sowie Vorbeugung gegen die Verbreitung von Infektionen in Krankenhäusern.
Unser ärgster Feind – wir selbst
Viele der wirkungsvollsten Maßnahmen, die wir anwenden könnten, sind bereits in unserer Hand (siehe die unten aufgeführten praktischen Schritte); es geht nur darum, dass wir alle sie konsequent anwenden. Um dies zu tun, müsste jeder und jede von uns mit echtem Verantwortungsgefühl handeln, da wir alle Bürger dieser Welt sind, die uns anvertraut ist.
Zaman bezeichnet Mikroben als „mikroskopische, aber machtvolle Lebensformen, die ebenso leicht genau den Körper schädigen können, in dem sie leben“. Einen Erreger unter dem Mikroskop zu identifizieren und unser Bestes zu tun, um ihn zu eliminieren, ist nur ein Teil der Herausforderung. Ihrer Verbreitung vorzubeugen, erfordert, dass wir uns mit unseren Gewohnheiten, Werten, Vorschriften und konkurrierenden Interessen auseinandersetzen.
Warum untergraben wir so oft unsere eigenen Fortschritte? Wir haben die Wirksamkeit von Antibiotika durch Missbrauch geschwächt und jetzt haben wir zu kämpfen, um der Falle zu entkommen, die wir uns selbst gestellt haben. Dieses Muster wiederholt sich immer wieder: in kurzfristigem Denken, das künftiges Wohl für gegenwärtige Annehmlichkeit opfert, in Wirtschaftssystemen, die Profit über Verantwortung stellen, in unserer Unfähigkeit, konsequent verantwortungsvoll zu handeln, selbst wenn wir wissen, was es kostet, das nicht zu tun.
Der Fortschritt der Wissenschaft geht immer weiter, aber Technologie allein war nie unsere Einschränkung. Die Frage ist, ob wir auf Dauer der Verpflichtung gerecht werden, die solche Lösungen uns abverlangen.
Praktische Schritte, um die Ausbreitung antimikrobieller Resistenzen zu verlangsamen
Bei dem Bemühen um einen Rückgang des unnötigen Einsatzes von Antibiotika ist Ausgewogenheit gefragt. Wer bei schweren bakteriellen Infektionen solche Mittel braucht, muss unkompliziert Zugang zu ihnen haben. Eine Minderung des unnötigen Einsatzes von Antibiotika hilft, zu verhindern, dass sie ihre Wirksamkeit zur Bekämpfung von Infektionen verlieren.
Organisationen wie die National Foundation for Infectious Diseases, das US Centers for Disease Control und der britische National Health Service bieten einige praktische Tipps an:
- Begreifen Sie, dass Missbrauch Resistenzen verursacht. Und nicht unser Körper wird immun gegen die Wirkstoffe – es sind die Bakterien selbst, die Resistenzen gegen die Antibiotika entwickeln. Was wir tun, hat Auswirkungen für alle.
- Nehmen Sie Antibiotika nur auf ärztliche Anweisung. Gegen Virusinfektionen wie Erkältung oder Grippe sind sie nicht wirksam. Ein Test kann helfen, zwischen Virus- und bakteriellen Infektionen zu unterscheiden.
- Halten Sie sich genau an die ärztlichen Anweisungen; nehmen Sie Medikamente genauso wie verordnet und genauso lange wie verordnet, selbst wenn Sie schon eine Besserung spüren.
- Heben Sie übrig gebliebene Antibiotika nicht für später auf.
- Teilen Sie Antibiotika nicht mit anderen Leuten.
- Beugen Sie Infektionen vor. Dazu gehört richtige Hygiene, häufiges Händewaschen, Zugang zu sauberem Wasser, Daheimbleiben, um nicht andere anzustecken, und sich impfen zu lassen, wenn es sinnvoll ist.
- Verringern Sie das Risiko von Lebensmittelvergiftungen, indem Sie beim Umgang mit Lebensmitteln und bei der Zubereitung von Speisen auf Sicherheit achten.
- Wenn Sie Tiere zu versorgen haben, setzen Sie Antibiotika nur ein, um bakterielle Infektionen zu behandeln.
- Sprechen Sie mit Freunden und Angehörigen über Antibiotikaresistenzen, um zu mehr Bewusstheit beizutragen.

